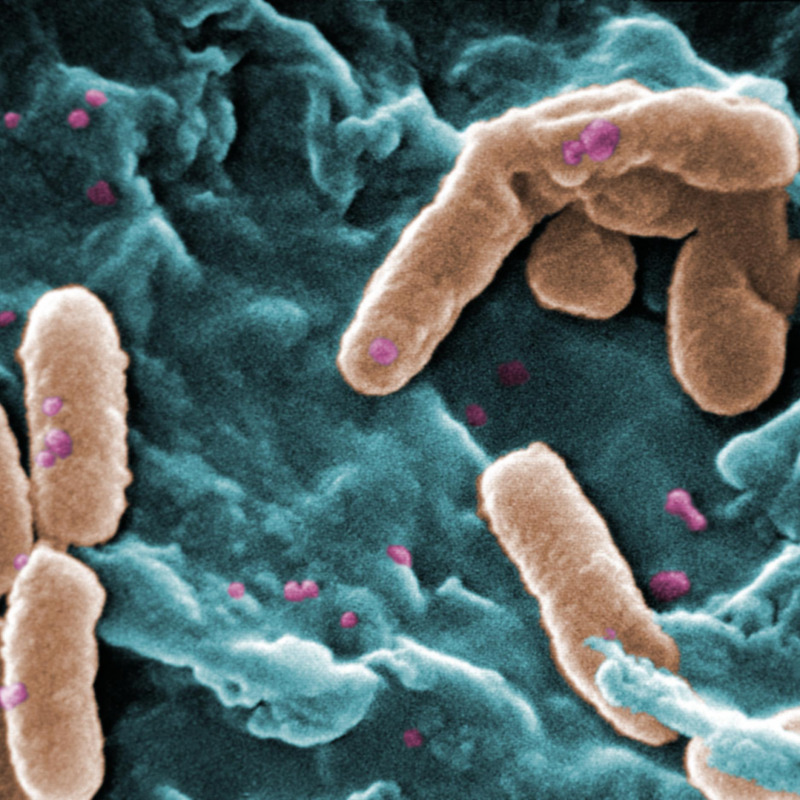
MILANO. È stato 'hackerato' per la prima volta un batterio che vive nel corpo umano: è il Bacteroides thetaiotaomicron, uno dei più comuni 'abitanti' dell'intestino.
I ricercatori del Massachusetts Institute of Technology (Mit) di Boston ne hanno preso il controllo riprogrammando il suo Dna con le più avanzate tecniche di biologia sintetica: in questo modo lo hanno trasformato in una versione '2.0' dotata di sensori, memoria e circuiti artificiali che in futuro potranno essere usati per diagnosticare e curare in loco patologie come il tumore del colon o le malattie infiammatorie intestinali.
Il risultato, descritto sulla rivista Cell Systems, apre la strada alla riprogrammazione a scopo diagnostico e terapeutico sia della flora batterica intestinale sia degli altri batteri 'buoni' presenti nel corpo umano.
La chiave sta nell'inserire le giuste 'istruzioni' nel Dna di questi microrganismi: gli esperti di biologia sintetica del Mit lo hanno fatto usando le più avanzate tecniche di manipolazione genetica, come ad esempio la discussa Crispr che consente la 'riscrittura' del genoma e recentemente utilizzata in Cina su embrioni umani. In questo modo sono riusciti a dotare il
batterio B. thetaiotaomicron di quattro geni 'sensori' che si accendono o spengono in risposta a stimoli esterni, che possono essere particolari sostanze contenute nel cibo ingerito oppure molecole 'spia' di una malattia in evoluzione. Per 'ricordare' le informazioni, al batterio è stata data una memoria genetica: questo grazie ad una classe di proteine, note come ricombinasi, che sono capaci di 'registrarè i dati raccolti scrivendoli direttamente sul Dna del batterio.
Per verificare che la trasformazione fosse avvenuta con successo, i ricercatori hanno provato a trasferire il batterio riprogrammato in un topo da laboratorio. Qui il microrganismo si è ambientato perfettamente, colonizzando l'intestino, ed è subito entrato in azione, riuscendo a 'fiutare' e ricordare quello che il topo aveva mangiato.
«Il nostro prossimo obiettivo - spiega il ricercatore Timothy Lu - è quello di dare questi strumenti genetici ad una vasta gamma di batteri che vivono da commensali nell'intestino umano». Questo perchè la composizione della flora intestinale varia da persona a persona, e i microrganismi che sono rari in un paziente potrebbero essere più abbondanti in un altro. Il secondo passo sarà quello di mettere a punto circuiti genetici più complessi che permettano di fare diagnosi più elaborate e precise, in modo da scatenare una risposta (come il rilascio di farmaci) solo quando sono presenti più campanelli d'allarme.








Caricamento commenti